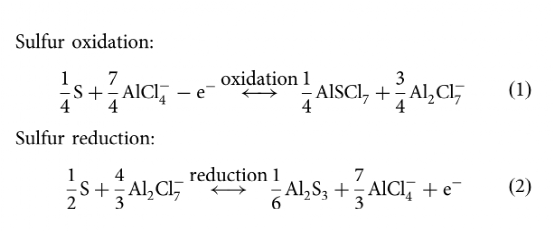硫含量丰富,具有较高的理论容量,作为电极材料可与金属阳极耦合,并与金属阳离子进行电化学还原,形成金属硫化物。尽管基于硫磺还原的比容量很高,但这些硫化物反向氧化成硫磺需要克服一个高能量屏障,导致过电位大,可逆性差。此外,硫的还原发生在低电化学电位下(与标准氢电极相比,约1.0V),并导致金属硫电池的低操作电压。例如,基于硫磺还原的Al-S电池通常表现出约0.5V的超低电池电压。因此,有限的可逆性和低电化学电位是硫磺电极实际使用的主要障碍。许多人都致力于通过适当的硫磺主机设计和电解质工程来改善金属硫磺电池的可逆性。然而,这些先前的尝试未能从根本上解决金属硫电池的低电压问题,因为电池的电压是由硫的氧化还原途径决定的,但这些努力并没有改变硫的还原途径。因此,基于硫磺还原的电池在高电压应用方面仍然远远不能令人满意。研究新的硫的氧化还原途径以实现金属硫电池的可行应用是非常重要的。在这方面,硫的氧化是一个值得考虑的途径,因为它可以弥补硫还原的内在低电压缺陷。
考虑到硫元素的多价性(-2、0、+2、+4、+6),硫可以被氧化成高价的硫化合物。不幸的是,硫的氧化过程很少被研究。由于硫的惰性,需要施加高电压来驱动其电化学氧化。这通常会伴随着电解质的分解,导致可逆性差。同时,硫的电化学氧化会经历一个与阴离子有关的电子损失过程。金属硫磺电池中常见的阴离子,如双(三氟甲基)磺酸盐、六氟磷酸盐都是弱氧化剂,不能将硫氧化成高价硫化合物。因此,在电化学稳定的电解质中具有强氧化力的阴离子是必要的,以高度可逆的方式氧化硫,但这一概念还没有被探索出来。
工作介绍
本工作首次证明了硫在AlCl3/碳酰胺离子液体中的可逆氧化。AlCl4-阴离子可以氧化硫,形成氯化硫化铝(AlSCl7),它可以被可逆地还原成硫,效率高达~94%。这种氧化-还原过程在广泛的高电化学电位范围内是可行的。受益于高可逆性和高电化学电位,铝-S电池可以在~1.8V左右稳定运行200次,这是迄今为止报告的铝-S电池的最高运行电压。与此形成鲜明对比的是,以前研究的基于硫磺还原的铝-S电池只能运行几十个循环,运行电压低得多,为~0.5V。这项工作为了解硫化学提供了新的线索,并提出了硫氧化是实现金属硫电池高电压应用的新途径。
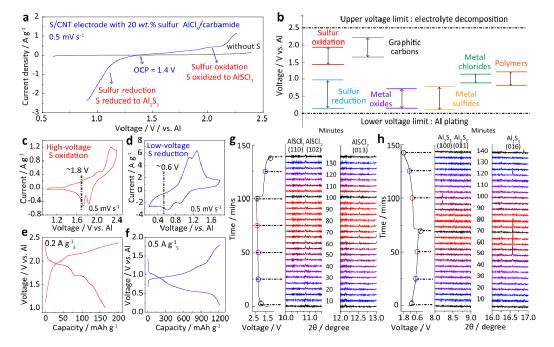
图1 硫在离子液体中的电化学氧化和还原。
在电化学硫磺氧化过程中AlSCl7的演变:
图1a显示了硫/碳纳米管(S/CNT)复合阴极在AlCl3/碳酰胺电解质中的线性扫描伏安法(LSV)曲线。在常用的AlCl3/1-乙基-3-甲基咪唑氯化物电解质中,硫在高氧化电压下并不稳定。S/CNT中的硫含量为20wt.%,AlCl3与碳酰胺的摩尔比为1.3:1。图1a中观察到的电流密度高于~2.0V,低于~1.0V,分别对应于硫的电化学氧化和还原。图1b总结了不同材料的电化学电位,本工作中硫的氧化电位远远高于以前报道的大多数材料。
循环伏安法(CV)曲线的比较显示了硫的氧化和还原的整体过程。从硫到AlSCl7的电化学氧化从~2.0V开始,而从AlSCl7到硫的反向还原在~1.8V发生(图1c)。对于硫的还原(图1d),硫在~1.0V以下开始被还原成硫化物。硫氧化的电化学电位要比还原的电位高得多。在静电充电-放电曲线中可以清楚地看到这种电位差。硫的氧化呈现出明显的高放电电压,约1.8V(图1e)。然而,硫的还原只显示了一个低得多的操作电压~0.5V(图1f)。
原位同步辐射X射线衍射(XRD)(图1g,h)。元素硫、Al2S3和AlSCl7是正方体、六方体和单斜体晶体,空间群分别为Fddd、P61和Pc。在硫的氧化过程中,正方体的硫转化为单斜体的AlSCl7,而在还原过程中,硫被还原为六方体的Al2S3。具体来说,对于硫的氧化过程(图1g),当Al-S电池被充电到2.4V时,分配给AlSCl7的(102)、(013)和(110)面的峰就会相继出现。对于从AlSCl7到硫磺的反向过程,那些分配给AlSCl7的峰逐渐消失,只有硫磺的特征峰保留。应该注意的是,在10.8°的衍射峰为硫的特征峰,由于硫的不完全电化学氧化,它在充电-放电过程中仍然存在。上述证据证实了硫磺到AlSCl7的有效电化学氧化,以及从AlSCl7回到硫磺的可逆性。
在硫还原过程中(图1h),Al2S3的(011)和(016)衍射峰分别出现在8.5和16.6°。对于反向过程,由于Al2S3转化为硫磺,这些峰逐渐消失。然而,在电荷过程中也可以发现Al2S3的(100)和(016)特征峰,这是由于Al2S3难以可逆地分解为硫。AlSCl7和Al2S3也都被不同截止电压下的XRD图所验证。上述证据证实了硫的氧化和还原化学作用,它分别基于AlSCl7和Al2S3的产物。
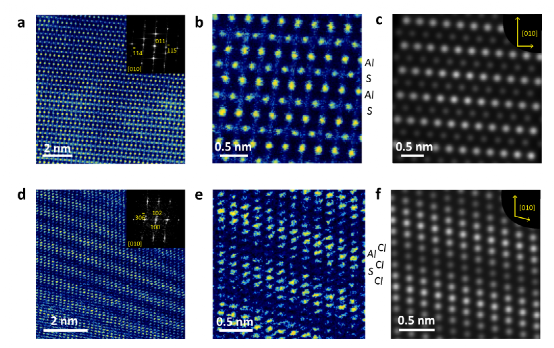
图2 硫的还原和氧化产物的显微图像。
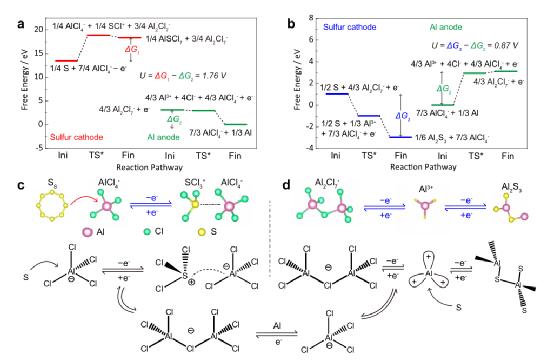
图3 硫氧化和硫还原反应途径的理论计算结果。
反应途径的理论计算:
密度函数理论(DFT)模拟了硫与AlCl4和Al2Cl7-阳离子之间的相互作用。对于硫的氧化过程(图3a),AlCl4-将S氧化成AlSCl7solid并伴随着电子的失去(公式1)。同时,Al2Cl7-被还原成AlCl4-,铝阳极上镀有铝。吉布斯自由能(ΔG)的变化可以通过使用电子转移数(n)和电化学势的差异(ΔU)来计算。在单电子转移的情况下,阴极和阳极之间的ΔG之差就是操作电压。正如预期的那样,硫的氧化表现出~1.76V的高电压,这与实验观察到的~1.8V是一致的(图1c)。对于硫的还原过程,硫被Al2Cl7-阳离子还原,形成Al2S3(公式2),同时,AlCl4-与Al阳极相遇,形成Al2Cl7-。基于硫还原的电压只有~0.87V(图3b),比硫氧化的电压低得多。此外,从AlSCl7到S的反向还原只需要克服0.52 eV的能量屏障,如图3a中红线的上坡计算。然而,从Al2S3到S的能垒却高达3.98 eV(图3b中的蓝线)。这一比较表明,从AlSCl7到S的逆向转化很容易,因此硫的氧化-还原过程的可逆性更好。图3c,d示意性地比较了硫的氧化和还原过程。AlCl4和Al2Cl7离子分别作为与硫发生反应的氧化剂和还原剂,而Al阳极被用作参比电极,与这些氧化还原反应配对以实现电荷平衡。硫的氧化和还原的途径总结如下。
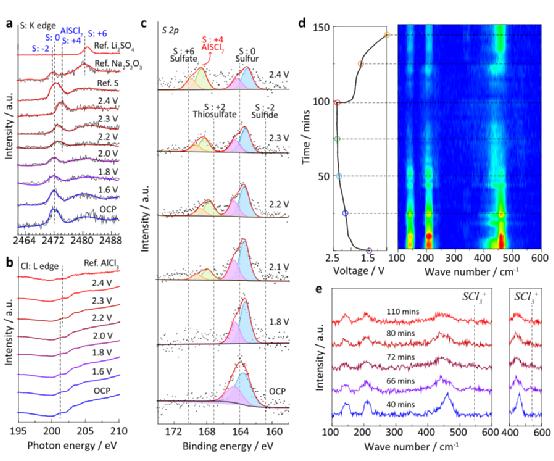
图4 通过光谱分析鉴定硫的氧化中间产物。
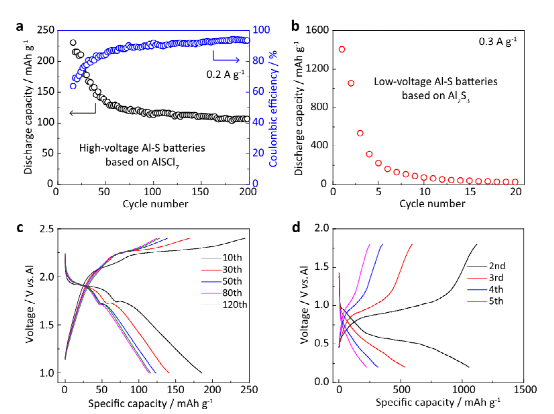
图5 铝-S电池中的硫氧化。
文章要点
一、证明了硫可以在离子液体中以高可逆性进行电化学氧化。
二、通过原位同步分析、高分辨率显微镜图像、光谱分析和理论计算证实了反应途径、AlSCl7氧化产物和SCl3+中间产物。
三、从硫磺到AlSCl7的电化学氧化是高度可逆的,CE%约为94%,而且氧化过程在广泛的电化学电位范围内是可行的。
四、基于硫氧化过程的铝-S电池可以在~1.8V左右稳定地运行200次,这是铝-S电池的最高运行电压。预计硫磺氧化过程可以与其他金属阳极耦合,用于各种金属硫磺电池,而不仅限于铝-S电池。
五、这项工作对硫化学有了新的认识,并显示了硫氧化途径对于设计可行的高压金属硫电池的巨大优势。
Reversible electrochemical oxidation of sulfur in ionic liquid for high-voltage AlS batteriesNature Communications ( IF 14.919 ) Pub Date : 2021-09-29, DOI: 10.1038/s41467-021-26056-7Huan Li, Rongwei Meng, Yong Guo, Biao Chen, Yan Jiao, Chao Ye, Yu Long, Anton Tadich, Quan-Hong Yang, Mietek Jaroniec, Shi-Zhang Qiao
第一作者:Liu Huan
通讯作者:乔世璋
单位:Adelaide大学
来源: |电化学能源 ID:easybattery007
 电池交流
电池交流 电池技术
电池技术 电池问答
电池问答 供求信息
供求信息 电池回收
电池回收 认证检测
认证检测 电池管理系统
电池管理系统 电池修复
电池修复 广告发布
广告发布 锂电池
锂电池 动力电池
动力电池 锂离子电池
锂离子电池 磷酸铁锂电池
磷酸铁锂电池 三元锂电池
三元锂电池 18650锂电池
18650锂电池 锂电池厂家
锂电池厂家 钠离子电池
钠离子电池 新能源汽车
新能源汽车 电池会议
电池会议 电池展会
电池展会 商务活动
商务活动